哌柏西利中国上市,联合方案治疗乳腺癌效果如何?哌柏西利何时能进医保?
发布时间:2020-12-14 点击量: 次
哌柏西利是全球首个细胞周期蛋白依赖性激酶(CDK)4/6抑制剂,已获得中国药监局批准上市,商品名:爱博新。
适应症:用于治疗一线联合芳香化酶抑制剂治疗绝经后女性,激素受体阳性(HR+)、人表皮生长因子受体2 阴性(HER2-)局部晚期或转移性的乳腺癌。
用法用量:与食物或芳香化酶抑制剂一起口服;建议起始剂量为125mg,每日一次,服用21天后休息7天;.建议基于个人的安全性和耐受性,中断或减少剂量。
哌柏西利的副作用
腹泻、血小板减少、 恶心、呕吐、 口腔炎。
严重不良反应:
中性粒细胞减少症:常合并感染。
1. 升中性粒细胞数治疗:可服用维生素B6、非格司亭。
2. 治疗感染相关症状
3. 对于中性粒细胞数严重减少者,出现发热应立即住院治疗。
4. 对于严重感染患者,还可给予中性粒细胞输注。
联合用药及治疗效果
1. 哌柏西利联合来曲唑一线治疗雌激素受体阳性HER2阴性晚期乳腺癌,可以显著延长患者的无进展生存期。一项II期临床研究表明,雌激素受体阳性转移性乳腺癌患者在合并使用哌柏西利与来曲唑时,其无进展生存期平均为20.2个月,相比之下,单独使用来曲唑的患者仅为10.2个月。
2. 哌柏西利联合氟维司群二线治疗对内分泌治疗耐药的雌激素受体阳性HER2阴性转移性乳腺癌,可以显著延长患者的无进展生存期。辉瑞哌柏西利的一项III期试验显示,接受哌柏西利与阿斯利康氟维司群(Faslodex)合并用药治疗的患者中位无进展生存期为9.2 个月,相比之下,以氟维司群加安慰剂治疗的患者中位无进展生存期仅为3.8个月。
2020版《中国临床肿瘤学会乳腺癌(CSCO BC)诊疗指南》发布。
新指南优化了治疗方案,在激素受体阳性(HR+)晚期乳腺癌患者的内分泌治疗策略上,将CDK4/6抑制剂(细胞周期素依赖性激酶)从II级推荐,提升至I级推荐。CDK4/6抑制剂类药物代表为哌柏西利。
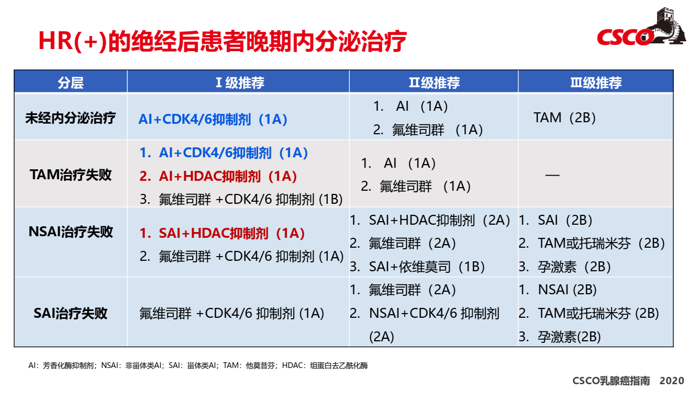
HR(+)的绝经后患者晚期内分泌治疗更新:
(1)未经内分泌治疗的患者,AI(芳香化酶抑制剂)+CDK4/6抑制剂成为I级推荐。
(2)他莫昔芬治疗失败的患者,AI/氟维司群+CDK4/6抑制剂成为I级推荐,新增AI+HDAC抑制剂为I级推荐。
(3)AI治疗失败细化为非甾体(NSAI)和甾体AI(SAI)治疗失败。NSAI治疗失败的患者中,SAI+CDK4/6抑制剂调整为I级推荐,新增SAI+HDAC抑制剂为I级推荐,SAI+依维莫司为II级推荐。
(4)SAI治疗失败的患者中,氟维司群+CDK4/6抑制剂调整为I级推荐,新增NSAI+CDK4/6抑制剂为II级推荐。
哌柏西利已在国内上市,但是还未进入医保,不过,哌柏西利仿制药也将在国内上市了,据海得康医学顾问了解到,碧康制药生产的Palbonix是哌柏西利是获得孟加拉政府监管机构批准合法生产的仿制药。质优价廉,国内患者能吃得起,仿制药着实让普通家庭受益。

孟加拉碧康生产的哌柏西利(帕博西尼)仿制药——Palbonix

