FDA批准calaspargase pegol-mknl治疗急性淋巴细胞白血病
发布时间:2019-05-31 点击量: 次
FDA批准calaspargase pegol-mknl治疗急性淋巴细胞白血病 急性淋巴细胞白血病(ALL)发生和起源于造血干细胞,其具体发病因素至今没有被人类完全掌握,不过几乎所有的ALL都有基因突变情况的发生,这就给calaspargase pegol-mknl等药物的治疗提供了依据。
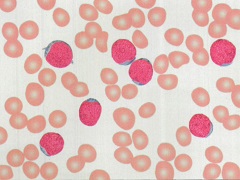
当calaspargase与多药化疗一起使用时,结果显示124名患者中的123名(99%,95%CI,96-100)在第6,12,18,24和30周维持NSAA> 0.1 U / mL 。推荐剂量为2500单位/平方米,静脉注射不超过每21天一次。
与该药物相关的最常见(≥10%)≥3级不良反应是转氨酶升高,胆红素升高,胰腺炎。根据美国食品和药物管理局的数据,在一项随机试验中,每3周施用的calaspargase pegol-mknl的安全性与每2周施用的pegaspargase相似。
calaspargase pegol-mknl是一种天冬酰胺特异性酶,对于儿童和成年患者都能起到明显治疗作用,患者可以在坚持服药之后获得症状的改善并杀死肿瘤细胞。凭借安全可靠的治疗效果,calaspargase pegol-mknl已经被FDA认定为急性淋巴细胞白血病的孤儿药。

